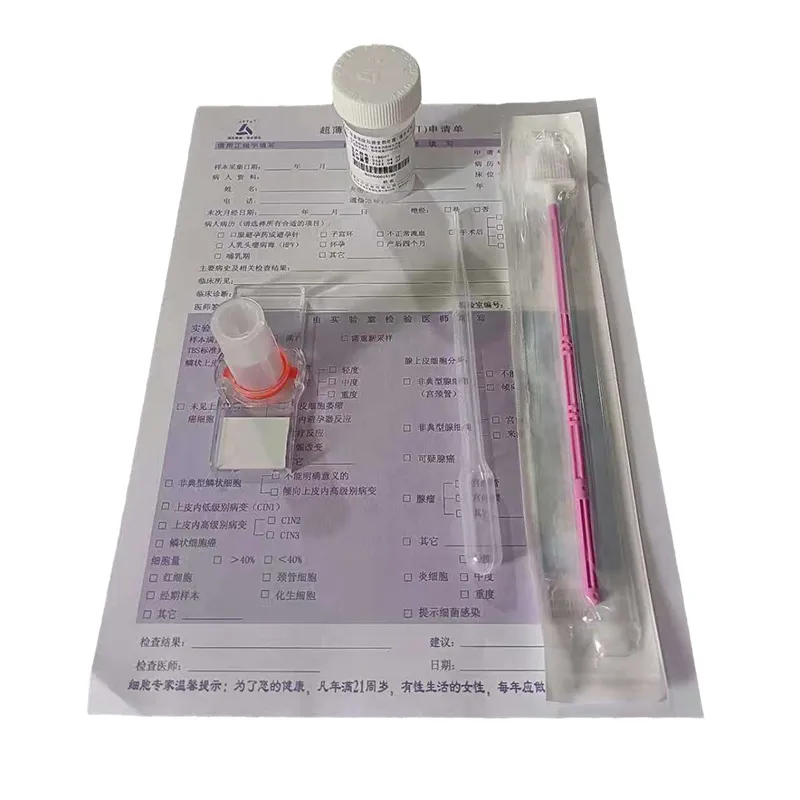
Цитологическая консервирующая жидкость для мокроты
Вот о чём часто забывают: цитологическая консервирующая жидкость для мокроты — это не универсальный ?консервант?, а ключевой фактор, определяющий, увидишь ли ты потом в микроскоп клетки или бесформенный детрит. Многие лаборатории, особенно те, что только переходят на жидкостную цитологию, думают — взял первую попавшуюся, залил, и порядок. А потом удивляются, почему морфология ?плывёт? или бактериальная флора забивает всё поле зрения. На деле, выбор и работа с этой жидкостью — это целая практическая дисциплина.
Что на самом деле скрывается за формулировкой ?консервирующая??
Когда я только начинал работать с мокротой по жидкостной методике, тоже считал, что главная функция — просто сохранить материал при транспортировке. Отчасти это так, но лишь отчасти. Хорошая жидкость должна выполнять минимум три задачи: немедленно фиксировать клетки, чтобы остановить аутолиз, лизировать эритроциты и частично слизь, и подавлять рост посторонней микрофлоры. Если какой-то компонент ?проседает? — проблемы гарантированы. Например, сталкивался с партией, где, видимо, сэкономили на антимикробном агенте — образцы через пару дней в пути приходили с запахом и агрессивным бактериальным фоном, который мешал оценке.
Здесь важно понимать разницу между фиксацией и консервацией. Фиксация — это быстрое ?замораживание? структуры клетки. Для мокроты, где клетки могут быть довольно хрупкими, это критически. Некоторые коммерческие жидкости делают упор на консервацию для долгого хранения, но с замедленной фиксацией. В итоге — потеря деталей ядра. Нужно смотреть состав: присутствует ли, например, метанол или его производные для быстрой фиксации, или же основа — альдегидные соединения для долгой консервации. Для рутинного скрининга туберкулёза или онкопатологии лёгких я всё же склоняюсь к вариантам с быстрым фиксирующим действием.
И ещё один нюанс, о котором редко пишут в инструкциях — вязкость самой мокроты. Густая, вязкая мокрота плохо смешивается с жидкостью, образует сгустки. Иногда приходилось в протокол добавлять этап предварительного аккуратного перемешивания образца с жидкостью в контейнере до отправки в аппарат для приготовления препарата. Иначе на слайде получались ?пустые? зоны и сгустки плохо обработанного материала.
Практические ловушки и как их обходить
Одна из самых частых проблем — несоответствие объёма жидкости объёму мокроты. Стандартно рекомендуют соотношение 1:3, но кто видел, как пациент откашливает ?стандартный? объём? Если материала мало, а жидкости много — клетки ?разводнятся?, их будет сложно найти на слайде. Если мокроты много, а жидкости мало — фиксация будет неполной, плюс риск микробного роста. Мы в лаборатории после нескольких неудач ввели правило: визуально оценивать объём и, если он явно больше 5 мл, делиться на два контейнера. Да, это удорожание, но зато сохранность материала.
Время до обработки — отдельная история. Производители пишут ?до 30 дней при комнатной температуре?. Технически, возможно. Но на практике я бы не стал держать образец для тонкослойной цитологии дольше недели. Особенно если в жидкости нет сильных стабилизаторов ДНК. Видел, как через две недели хранения в неидеальных условиях (скажем, в приёмном отделении, где может быть жарко) в клетках появлялись артефакты, напоминающие дистрофические изменения. Это может сбить с толку цитолога.
И конечно, совместимость с автоматическим препарированием. Не всякая жидкость одинаково хорошо работает с разными тонкослойными цитологическими мазок-препараторами. Была ситуация, когда мы тестировали новую, более дешёвую жидкость на старом оборудовании. Аппарат постоянно забивался — видимо, из-за иного поверхностного натяжения или размера частиц после лизиса. Пришлось вернуться к проверенному варианту. Это к вопросу о том, что менять реагенты ?на лету? без валидации в своих условиях — прямой путь к браку в работе.
Связь с оборудованием и экосистемой лаборатории
Сегодня мало выбрать просто жидкость. Нужно смотреть на неё как на часть системы. Вот, например, компания ООО Хубэй Тайкан Медицинское Оборудование (сайт: https://www.cnhbtk.ru) позиционирует себя как специалиста по комплексному обновлению патологических лабораторий. Это важный момент. Их подход — это не просто продать тебе реагент, а предложить связку: консервирующая жидкость + совместимые с ней препарирующие системы + иногда даже протоколы окрашивания. Когда все компоненты от одного производителя и оптимизированы друг под друга, это снижает количество ?необъяснимых? артефактов.
В их нише — экологическое и интеллектуальное обновление лабораторий — это означает, что и к жидкостям, вероятно, предъявляются требования по безопасности (низкая летучесть, нетоксичность) и удобству интеграции в LIS-системы (чёткие штрих-коды, стабильные партии). Для крупной лаборатории, которая делает сотни образцов мокроты в неделю, такие вещи не менее важны, чем цитологическое качество. Потому что сбой в логистике или проблемы с идентификацией образца сведут на нет всю точность микроскопа.
Я знакомился с их портфелем — они делают акцент на реагентах для раннего скрининга, включая онкологию. Это накладывает отпечаток и на продукты для мокроты. Можно ожидать, что их цитологическая консервирующая жидкость разработана с оглядкой на последующее возможное молекулярное тестирование (сохранность нуклеиновых кислот). Это уже следующий уровень, не просто морфология. Хотя для рядовой лаборатории, занимающейся, скажем, диагностикой туберкулёза, это может быть избыточно.
Личный опыт и субъективные предпочтения
За годы работы руки привыкли к определённым маркам. Есть жидкости, после которых образец приходит как ?прозрачный?, с минимальным количеством детрита, и клетки лежат красивым монослоем. А есть — после которых словно каша, приходится долго искать. Субъективно, мне нравятся жидкости с добавлением мягких муколитиков. Они не так агрессивно разрушают всё, но эффективно справляются со слизью, что для мокроты архиважно.
Один раз попробовал сэкономить и использовать для мокроты жидкость, заявленную как ?универсальная для всех биоматериалов?. Не рекомендую. Для гинекологических образцов она, может, и хороша, но вязкая мокрота — совсем другая среда. Получил плохое качество препаратов и больше не экспериментировал. Вывод: специализация важна. Для мокроты — свой, для мочи — свой, для соскобов — свой. Универсальных солдатиков не бывает.
Цвет жидкости — мелочь, но важная. Бесцветную я не люблю. Легко перепутать с водой или другим реагентом. Предпочтительнее слабо окрашенные, например, жёлтые или розовые. Это простая визуальная подсказка на этапе приёмки и обработки, что в контейнере есть консервант.
Взгляд в будущее: куда движется технология?
Сейчас тренд — это интеграция с автоматическим скринингом и ИИ. Соответственно, требования к консервирующим жидкостям меняются. Нужна не просто сохранность морфологии, а максимальная стандартизация результата, минимум артефактов, которые алгоритм может принять за патологию. Думаю, в ближайшие годы мы увидим появление жидкостей, формула которых будет заточена именно под цифровую цитологию — с ещё более стабильной фиксацией и контрастностью.
Второе направление — экологичность. Утилизация использованных консервирующих жидкостей, часто содержащих метанол или формальдегидные производные, — это головная боль для лаборатории. Разработка более безопасных, но не менее эффективных формул — это вызов для производителей вроде ООО Хубэй Тайкан, которые заявляют об ?экологическом обновлении?. Возможно, будущее за растворами на основе нетоксичных полимеров.
В итоге, возвращаясь к началу. Цитологическая консервирующая жидкость для мокроты — это не расходник, а полноценный реагент, от которого на 50% зависит результат. Её выбор нельзя делегировать отделу закупок только по критерию цены. Нужно тестировать в своих условиях, на своём оборудовании, смотреть на морфологию, на стабильность партий, на логистику. Это та самая ?мелочь?, которая отделяет качественную лабораторную диагностику от простой формальной отписки. И в этом контексте подход компаний, которые думают о комплексной экосистеме для лаборатории, а не просто о продаже товара, выглядит всё более оправданным.
Соответствующая продукция
Соответствующая продукция
Самые продаваемые продукты
Самые продаваемые продукты-
 Гистокассеты для заливки и обработки
Гистокассеты для заливки и обработки -
 Криомикротом
Криомикротом -
 Архивные боксы для гистологических препаратов
Архивные боксы для гистологических препаратов -
 TP100A3.TP200A1
TP100A3.TP200A1 -
 Промывной раствор (безбензольный)
Промывной раствор (безбензольный) -
 Раствор для кислотоустойчивого окрашивания
Раствор для кислотоустойчивого окрашивания -
 Жидкость для подготовки гистологических образцов
Жидкость для подготовки гистологических образцов -
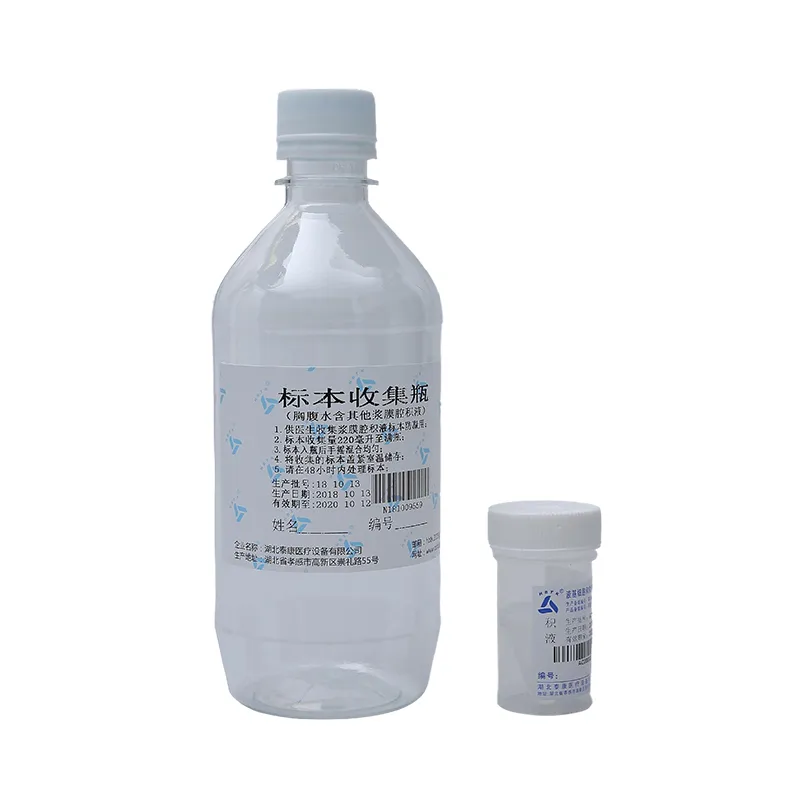 Специальная консервирующая жидкость для плеврального/асцитического выпота и лаважных жидкостей
Специальная консервирующая жидкость для плеврального/асцитического выпота и лаважных жидкостей -
 Ленточный тканевый дегидратор
Ленточный тканевый дегидратор -
 Просветляющая жидкость для препаратов (безбензольная)
Просветляющая жидкость для препаратов (безбензольная) -
 Раствор для окрашивания по Папаниколау
Раствор для окрашивания по Папаниколау -
 Фиксатор для тканей (альдегидсодержащий)
Фиксатор для тканей (альдегидсодержащий)
Связанный поиск
Связанный поиск- OCT-среда для заливки в криомикротоме
- Набор реагентов для раннего скрининга опухолей мочевыводящих путей
- Автоматический гистологический окрасчик
- Иммуногистохимия патологических тканевых срезов
- Экологические реагенты без альдегидов, бензола, кетонов
- ИГХ-антигены
- контейнер вакуумный для сбора образцов мочи
- взятия мазка на цитологическое исследование
- окраска цитологических мазков по папаниколау
- цитологическое исследование мазков с поверхности шейки матки