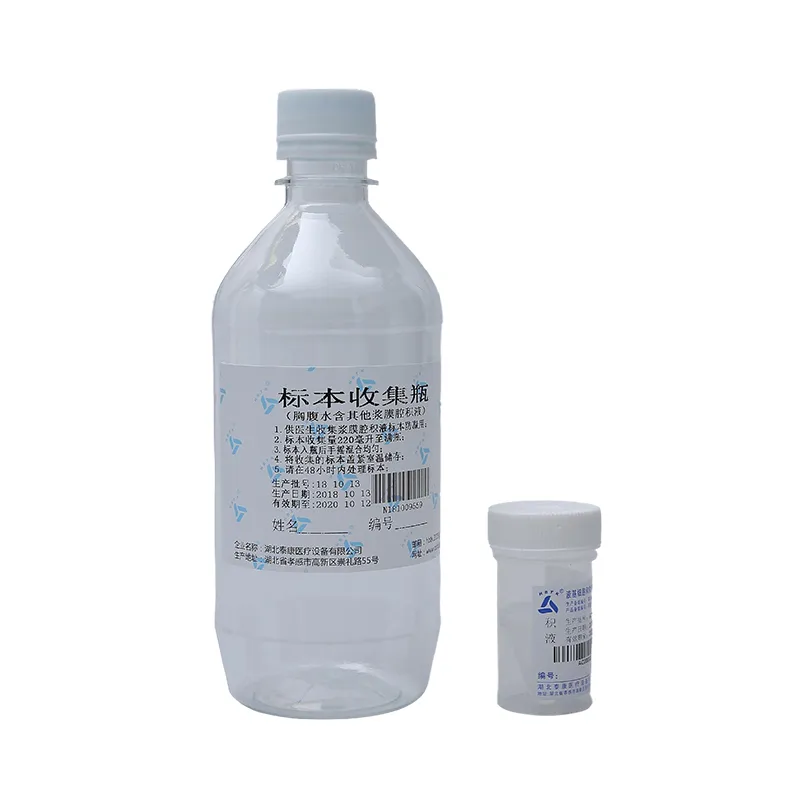
Пробирка для сбора вирусов
Когда говорят о пробирке для сбора вирусов, многие представляют себе обычную стерильную емкость. Вот тут и кроется первый, и довольно серьезный, пробел в понимании. Если бы все было так просто, мы бы не сталкивались с проблемой деградации РНК в образцах к моменту доставки в лабораторию или ложноотрицательными результатами из-за неактивных транспортных сред. Ключевое слово — ?транспортная среда?. Это не просто физический контейнер, это химико-биологическая система, задача которой — сохранить жизнеспособность и целостность вирусных частиц или их нуклеиновых кислот, а часто — инактивировать патоген для безопасности лаборанта. От выбора этой ?пробирки? на самом первом этапе зависит до 30% успеха всего последующего анализа. Я много раз видел, как в условиях аврала, особенно в начале пандемии, брали первую попавшуюся стерильную пробирку, а потом бились над слабым сигналом в ПЦР.
Из чего состоит ?правильная? пробирка: разбираем по полочкам
Итак, что мы имеем внутри? Основа — это буферная среда. Для вирусов с оболочкой, вроде гриппа или SARS-CoV-2, часто используют среды с белковыми стабилизаторами (например, БСА) и антибиотиками для подавления бактериальной флоры. Для ПЦР-диагностики критически важны ингибиторы нуклеаз, особенно РНКаз, которые есть везде, даже на коже персонала. Если их нет — РНК вируса начнет разрушаться в течение часов. Отсюда и требование к материалу пробирки: медицинский полипропилен, инертный, не сорбирующий нуклеиновые кислоты на стенки. Пробка — только винтовая, с гарантированной герметичностью. Резиновые пробки под давлением иглы иногда дают микрощели, что ведет к риску утечки аэрозоля и высыханию среды.
Еще один нюанс — объем транспортной среды. Стандарт — 2-3 мл. Но здесь есть подвох: при взятии мазка из носоглотки в пробирку часто погружают зонд с тампоном. Если зонд длиннее, чем высота столба жидкости, кончик с образцом остается сухим. Часть биоматериала не смывается, остается на тампоне и теряется. Приходилось инструктировать медсестер: ?Обязательно проверьте, чтобы жидкость покрывала наконечник зонда после погружения?. Казалось бы, мелочь, но из таких мелочей складывается точность.
И, конечно, маркировка. Матовая поверхность для надписей шариковой ручкой — обязательно. Глянец от маркера стирается. Мы как-то получили партию с глянцевыми этикетками — пришлось обматывать их лейкопластырем и подписывать поверх. Непрофессионально и риск перепутать образцы.
Практические ловушки и неудачный опыт
Один из самых показательных случаев был связан с закупкой ?экономичных? пробирок у нового поставщика. Все сертификаты были в порядке, но на практике... Внутри оказался гель-барьер (типа как в вакуумных пробирках для крови). Производитель утверждал, что он инертный и помогает стабилизировать среду. Однако при транспортировке в условиях тряски (доставка курьерской службой в отдаленные пункты) этот гель частично смешивался с транспортной средой. В лаборатории при центрифугировании перед выделением РНК этот гель давал осадок, который забивал мембраны в силикатных колонках. Выход нуклеиновых кислот падал катастрофически. Пришлось срочно менять протокол, вводить дополнительный этап фильтрации, что увеличивало время и стоимость анализа. Вывод: любое усложнение системы должно быть многократно апробировано. Классическая жидкая среда без лишних элементов часто надежнее.
Другая проблема — логистика и хранение. Транспортные среды часто требуют хранения при +4°C. А что происходит на складе в регионах летом? Или в машине курьера? Мы начали внедрять системы мониторинга температуры в транспортных боксах, но это удорожание. Иногда проще и правильнее использовать среды, стабильные при комнатной температуре, даже если они немного дороже. Экономия на пробирках может обернуться потерями на повторных заборах и недоверии клиницистов к результатам.
Связь с цитопатологией: где пересекаются миры
Хотя наша основная тема — вирусы, нельзя не отметить, что принцип сохранения лабильного биоматериала универсален. Компании, которые глубоко понимают эту проблему, часто успешны в смежных областях. Вот, например, ООО Хубэй Тайкан Медицинское Оборудование (сайт: https://www.cnhbtk.ru). Они изначально фокусировались на жидкостной цитологии, а это, по сути, та же задача: сохранить морфологию и биомолекулы клеток в жидкой среде при транспортировке в лабораторию. Их опыт в создании стабильных реагентов для тонкослойных цитологических мазков и скрининга рака шейки матки напрямую связан с глубокой проработкой химии консервирующих сред. Если компания умеет сохранить целостность ДНК человека в клетках эпителия для онкоскрининга, то и с транспортными средами для вирусной РНК у нее, вероятно, будет серьезный технологический бэкграунд. Это не просто производитель пластика, это специалист по преаналитике. Их позиционирование как компании для экологического и интеллектуального обновления лабораторий — это как раз про комплексный подход, где пробирка — часть системы.
Тренды и субъективные размышления о будущем
Сейчас явный тренд — переход к пробиркам с инактивирующей средой. Безопасность персонала выходит на первый план. Раньше часто брали образец в среду без инактивации, рискуя. Современные среды содержат детергенты, которые разрушают липидную оболочку вируса, но щадят РНК. Это уже стандарт для многих новых комплектов. Но и здесь есть нюанс: некоторые детергенты могут мешать последующим иммунохроматографическим тестам, если лаборатория планирует делать и ПЦР, и быстрые антигенные тесты из одной пробирки. Нужно четко понимать алгоритм.
Еще одно направление — пробирки с интегрированными тампонами. Все в одном: стерильный зонд уже находится внутри пробирки с нужным объемом среды. Открыл, взял мазок, поместил зонд обратно, отломил по насечке — и готово. Минимизирует ошибки оператора и риск контаминации. Но стоимость выше. Оправдано ли это в масштабах обычной поликлиники? Вопрос экономики и организации потока.
Лично я считаю, что следующим шагом станет ?умная? маркировка — не просто штрих-код, а RFID-метка, которая может записывать время взятия образца и температуру хранения. Но это пока из области футурологии для большинства лабораторий. Хотя, если говорить о компаниях вроде ООО Хубэй Тайкан Медицинское Оборудование, их фокус на интеллектуальном обновлении лабораторий как раз намекает, что подобные решения могут появиться быстрее, чем мы думаем. В конце концов, их работа в области раннего скрининга по моче тоже требует контроля преаналитики.
Заключительные штрихи: что остается за кадром
В суматохе часто забывают о человеческом факторе. Самая совершенная пробирка для сбора вирусов бесполезна, если медработник не обучен правильно ее использовать. Сколько раз приходилось видеть, как пробирку заполняют не до метки, перегружая средой, или, наоборот, недоливают. Или встряхивают после взятия образца, хотя протокол требует аккуратного вращения. Обучение, простые и понятные инструкции-пиктограммы на упаковке — это часть продукта. Производитель, который вкладывается в это, вызывает больше доверия.
И последнее. Никогда не экономьте на валидации. Получили новую партию пробирок — не поленитесь, поставьте параллельно несколько десятков образцов со старыми, проверенными, и сравните выход РНК и пороги цикла в ПЦР. Это скучно, отнимает время, но это единственный способ быть уверенным. Потому что в итоге в этой пробирке — не просто ?вирус?, а диагноз, решение о лечении и эпидемиологическая ситуация. И ответственность за то, чтобы первое звено в этой цепочке было прочным, лежит на всех нас: от производителя, вроде ООО Хубэй Тайкан Медицинское Оборудование, до лаборанта, принимающего образец.
Так что, возвращаясь к началу, пробирка — это далеко не просто трубка. Это фундамент. И к ее выбору нужно подходить с тем же вниманием, что и к выбору анализатора.
Соответствующая продукция
Соответствующая продукция
Самые продаваемые продукты
Самые продаваемые продукты-
 Одноразовые микротомные лезвия
Одноразовые микротомные лезвия -
 Фиксатор для тканей (альдегидсодержащий)
Фиксатор для тканей (альдегидсодержащий) -
 Раствор для окрашивания по Папаниколау
Раствор для окрашивания по Папаниколау -
 Промывной раствор (безбензольный)
Промывной раствор (безбензольный) -
 Нержавеющие гистологические заливочные матрицы
Нержавеющие гистологические заливочные матрицы -
 Просветляющая жидкость для препаратов (безбензольная)
Просветляющая жидкость для препаратов (безбензольная) -
 Нейтральная бальзамная смола
Нейтральная бальзамная смола -
 Микротом TKY-QPD (ручной)
Микротом TKY-QPD (ручной) -
 Раствор для окрашивания гинекологических мазков
Раствор для окрашивания гинекологических мазков -
 Среда для заливки в криостате
Среда для заливки в криостате -
 Жидкостный тонкослойный цитологический пресс
Жидкостный тонкослойный цитологический пресс -
 Ранний скрининг рака лёгких
Ранний скрининг рака лёгких
Связанный поиск
Связанный поиск- Набор расходных материалов и реагентов для скрининга опухолей мочевыводящих путей
- Одноразовые патологические расходные материалы
- Тонкослойная обработка цервикальных образцов
- Экспресс-тканевой дегидратор для патологии
- анализ цитологический мазок
- Селекция расходных материалов для окрашивания
- цитологический мазок атрофический
- в цитологическом мазке воспалительный процесс слизистой оболочки
- Жидкостный цитологический пресс-окрасчик-монтировщик
- Раствор для окрашивания гематоксилином-эозином