
Консервирующая жидкость для носоглоточных реагентов
Если вы думаете, что вся консервирующая жидкость для ПЦР-тестов одинаковая — вы глубоко ошибаетесь. На бумаге состав может казаться стандартным, но на практике, от партии к партии, от одного производителя к другому, возникают мелочи, которые могут съесть половину чувствительности анализа. Речь не о формальном соответствии ГОСТ или ТУ, а о том, что происходит с мазком через два часа в транспорте при +30°С или после недели хранения в холодильнике с перепадами температуры. Вот об этих ?неочевидных нюансах? и хочу порассуждать, исходя из того, что пришлось увидеть и попробовать самому в лабораторной практике.
Между теорией и пробиркой: где теряется стабильность?
Начну с банального. Все инструкции пишут: ?обеспечивает стабильность РНК/ДНК вируса при температуре 2–8°С до 7 суток?. Это в идеальном мире лабораторного холодильника с графиком валидации. А в реальности? Курьер задерживается, термоконтейнер греется на солнце, в пункте приёма холодильник перегружен и температура на полке +10°С. И вот здесь начинается самое интересное. Формально — условия нарушены, но сдавать пробу в утиль жалко. Запускаем в работу. И иногда — всё хорошо. А иногда — полный провал, внутренний контроль не отзывается.
Я долго думал, что дело в самом вирусе, в его количестве. Пока не начал сравнивать разные консервирующие жидкости в таких ?стрессовых? условиях. Брал один и тот же клинический материал, делил, помещал в среды от разных поставщиков и создавал им ?тяжёлую жизнь?: циклы заморозки-разморозки, нагрев до 25°С на 48 часов. Результаты по кинетике выделения нуклеиновых кислот потом смотрел на амплификаторе. Разброс был колоссальный. Одна среда держала удар, другая — нет, и вирусная РНК деградировала значительно быстрее.
Вывод, который напрашивается сам: ключевой параметр — это не только инактивация вируса (с чем справляются почти все), а именно буферная ёмкость системы и стабильность химических связей консервантов при неидеальных условиях. Некоторые составы, особенно на основе гуанидин-тиоцианата, казалось бы, должны быть ?крепче?, но на практике при длительном хранении в тепле давали повышенный фон и ингибирование ПЦР. Видимо, дело в примесях или в процессе стабилизации pH.
Кейс из практики: когда экономия на среде оборачивается переделками
Помню историю пару лет назад. Лаборатория, с которой мы сотрудничали, решила сэкономить и перешла на более дешёвые реагенты для носоглоточных мазков. Всё было хорошо первые два месяца. Потом пошли жалобы от клиник на ?сомнительные? результаты и случаи ложноотрицательных ответов у явно симптомных пациентов. Стали разбираться. Оказалось, что новая жидкость плохо переносила транспортировку в обычных, не охлаждаемых, контейнерах, которые использовались для срочных заборов на дому. При этом старый поставщик, тот же ООО Хубэй Тайкан Медицинское Оборудование, изначально предупреждал о необходимости строгого холодового режима для их состава, но зато предоставлял валидированные данные по стабильности именно в таких условиях. Экономия же вышла боком: пришлось переделывать десятки анализов, нести репутационные потери.
Этот случай заставил меня внимательнее изучать не только паспорт качества, но и протоколы валидации производителя. Важно, чтобы эти испытания включали не только идеальные сценарии. Компания ООО Хубэй Тайкан Медицинское Оборудование, к слову, в своих материалах всегда акцентирует внимание на комплексном подходе к стабильности преаналитики, что логично, учитывая их специализацию на цитопатологии и оборудовании для лабораторий. Для них консервирующая жидкость — это не просто буфер, а часть системы, обеспечивающей качество образца от момента забора до постановки в амплификатор.
Что я взял для себя из этой истории? Теперь всегда задаю вопросы: ?А что будет с пробой, если она пробудет в машине курьера 6 часов при +5°С? А при +15°С? Есть ли у вас данные по порогу ингибирования ПЦР после длительного хранения??. Ответы на эти вопросы часто куда информативнее, чем красивые графики в каталоге.
Вязкость, осадок и другие ?мелочи?, которые мешают роботу
Перейдём к чисто техническим моментам, о которых редко пишут в статьях, но которые ежедневно раздражают лаборантов. Вязкость консервирующей жидкости. Казалось бы, мелочь. Но если она слишком густая, автоматические пипетки дозируют с ошибкой, появляются пузыри, которые потом мешают при переносе пробы. Если слишком жидкая — есть риск разбрызгивания и перекрёстной контаминации. Идеальная консистенция — как у слегка разбавленного глицерина. У некоторых производителей она от партии к партии ?гуляет?.
Ещё один бич — образование осадка. Видел жидкости, которые после месяца хранения в холодильнике давали мелкодисперсный осадок. Фильтровать? Центрифугировать? Инструкция молчит. А этот осадок может забивать каналы автоматических станций для выделения или, что хуже, быть источником ингибиторов ПЦР. Приходилось эмпирически подбирать режим предварительного центрифугирования пробирок перед постановкой, что добавляло лишний этап в работу и риск для персонала.
Именно поэтому сейчас при выборе обращаю внимание не только на химический состав, но и на физические характеристики. Прошу предоставить пробную партию, чтобы ?пощупать? её в рабочих условиях на нашем оборудовании. Часто бывает, что заявленные для автоматических станций протоколы от производителя требуют тонкой подстройки под конкретную вязкость и смачиваемость жидкости.
Интеграция в лабораторный процесс: больше чем просто реагент
Важный аспект, который часто упускают — как консервирующая жидкость для носоглоточных реагентов встраивается в общий технологический цикл лаборатории. Это вопрос совместимости. Совместимости с тампонами-зондами (не все материалы наконечников инертны к некоторым консервантам). Совместимости с пробирками (пластик некоторых марок может адсорбировать компоненты среды). И, конечно, совместимости с последующими этапами — наборами для выделения и ПЦР-смесями.
У нас был опыт, когда мы использовали очень эффективную, судя по литературе, жидкость, но наши стандартные наборы для выделения на магнитных частицах стали давать низкий выход. Оказалось, что один из стабилизаторов в её составе конкурировал с частицами за связывание нуклеиновых кислот. Пришлось менять либо среду, либо протокол выделения. Это месяцы новой валидации.
Компании, которые думают системно, как ООО Хубэй Тайкан Медицинское Оборудование, предлагают часто не просто реагент, а готовое решение — пробирку с жидкостью, совместимую с определёнными типами зондов и протоколами. В их нише, цитопатологии, это вообще критически важно, ведь там работают с более хрупким клеточным материалом. Этот подход — thinking in systems — постепенно проникает и в область молекулярной диагностики. Жидкость перестаёт быть расходником, она становится ключевым звеном преаналитической цепочки, и её выбор должен быть таким же тщательным, как и выбор амплификатора.
Взгляд в будущее: что ещё можно улучшить?
Глядя на текущий рынок, вижу несколько точек роста. Первое — это универсальные среды, способные консервировать материал не только для ПЦР, но и, например, для иммунохроматографического экспресс-тестирования или культивирования. Пока что это чаще два разных мира. Второе — индикация. Было бы здорово иметь в составе жидкости пассивный индикатор, меняющий цвет при критическом нарушении температурного режима или при превышении срока хранения. Не как основной критерий, а как визуальную подсказку для курьера или лаборанта при приёмке.
И третье, самое, пожалуй, важное — экологичность. Некоторые составы на основе гуанидин-тиоцианата требуют особых мер утилизации. В условиях массового скрининга это становится серьёзной проблемой. Будущее, думаю, за более ?зелёными? формулами, которые не теряют в эффективности. Здесь, кстати, компании, позиционирующие себя как экологические, как раз Хубэй Тайкан в своей деятельности, имеют хороший задел для разработок.
В итоге, возвращаясь к началу. Выбор консервирующей жидкости — это не протокольное действие из инструкции. Это стратегическое решение, влияющее на всю цепочку от пациента до результата. Это постоянный компромисс между стоимостью, стабильностью, совместимостью и удобством работы. И самый ценный опыт здесь — не удачные партии, а как раз те проблемные случаи, которые заставляют копать глубже, задавать неудобные вопросы поставщикам и постоянно сверять теорию с практикой у лабораторной стойки. Только так можно найти тот самый состав, который будет работать не на бумаге, а в реальной жизни, со всеми её курьерами, перегруженными холодильниками и срочными пробами.
Соответствующая продукция
Соответствующая продукция
Самые продаваемые продукты
Самые продаваемые продукты-
 Предметные стекла с адгезивным покрытием
Предметные стекла с адгезивным покрытием -
 Микротом TKY-QPE (ручной)
Микротом TKY-QPE (ручной) -
 Парафиновые срезы для микротомии
Парафиновые срезы для микротомии -
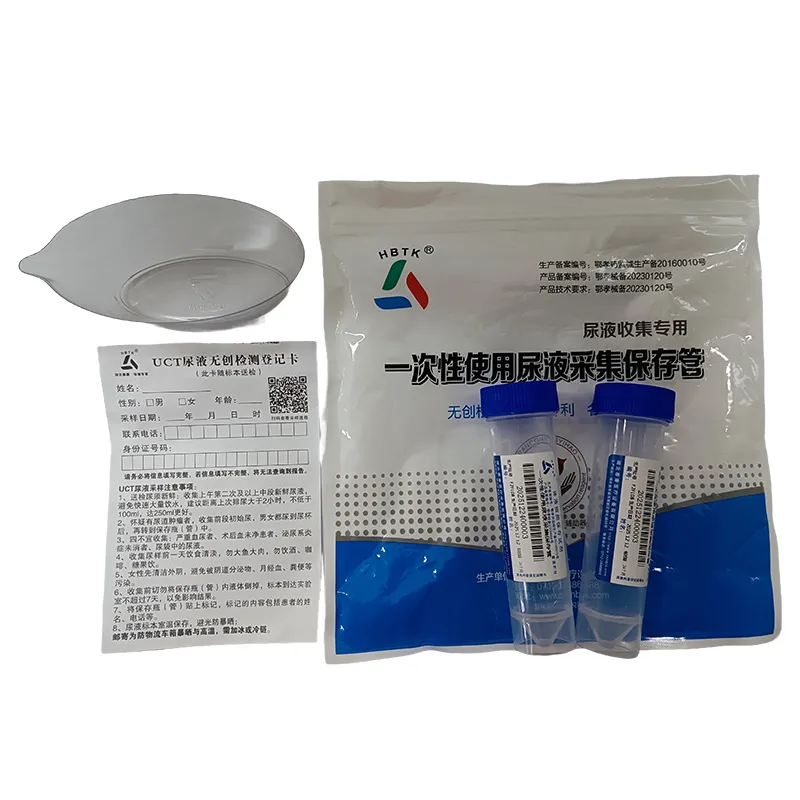 Неинвазивный ранний скрининг урологических опухолей
Неинвазивный ранний скрининг урологических опухолей -
 Комбинированный транспортный пакет для образцов (с альдегидом)
Комбинированный транспортный пакет для образцов (с альдегидом) -
 Ленточный тканевый дегидратор
Ленточный тканевый дегидратор -
 Парафиновый заливочный станок
Парафиновый заливочный станок -
 Стеллажи для окрашивания
Стеллажи для окрашивания -
 Просветляющая жидкость для препаратов (безбензольная)
Просветляющая жидкость для препаратов (безбензольная) -
 Пакеты для образцов
Пакеты для образцов -
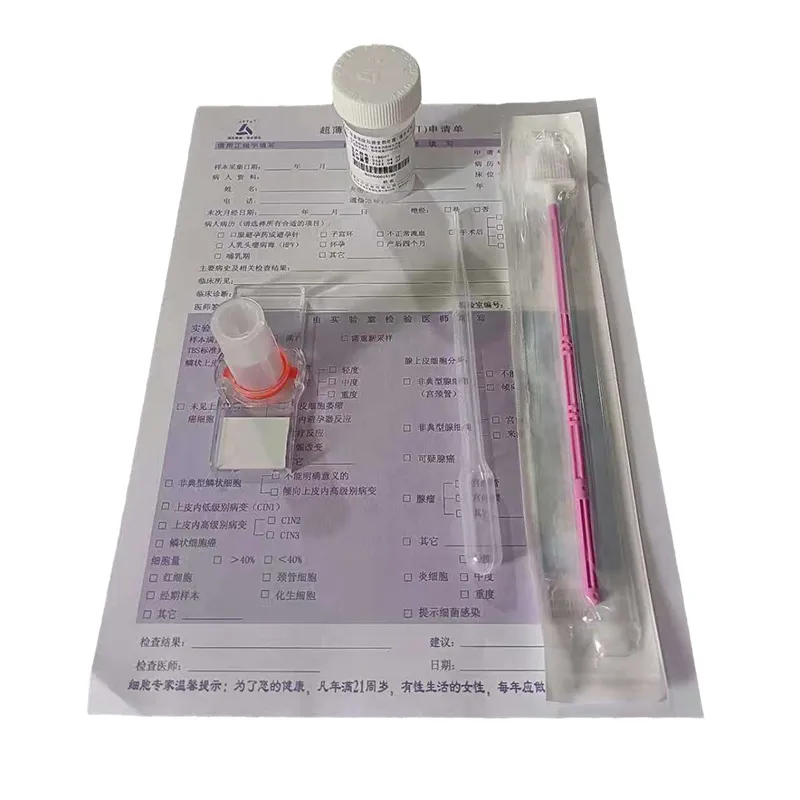 Жидкостная цитологическая консервирующая жидкость (гинекология)
Жидкостная цитологическая консервирующая жидкость (гинекология) -
 Раствор для окрашивания гинекологических мазков
Раствор для окрашивания гинекологических мазков
Связанный поиск
Связанный поиск- Гинекология
- цитологическое исследование атрофический тип мазка
- Ротационный ручной микротом
- Раствор для окрашивания по Папаниколау
- Патологические предметные стекла
- взятия мазка на цитологическое исследование
- Раствор для окрашивания гинекологических мазков
- Полностью автоматизированное жидкостное тонкослойное цитологическое оборудование
- цитологический мазок воспалительный тип мазка
- Контейнер для сбора образцов мокроты











