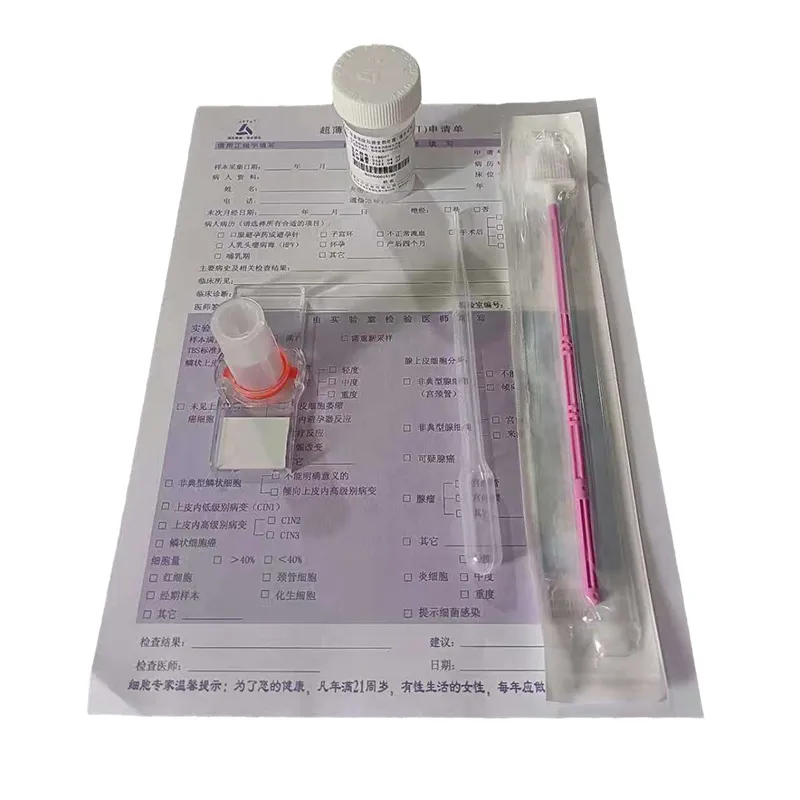
Забор материала для ВПЧ (гинекология)
Когда слышишь ?забор материала для ВПЧ?, многие сразу представляют стандартный мазок щёточкой — и всё. Но на деле, это как раз та точка, где скрининг может пойти не так, ещё до попадания материала в лабораторию. Видела достаточно случаев, когда идеальный по бумагам образец потом давал сомнительный результат, а причина крылась не в тест-системе, а в том, как брали и сохраняли этот материал. Часто упускают из виду, что забор материала для ВПЧ — это не просто механическое действие, а процедура, напрямую влияющая на чувствительность метода, особенно жидкостной цитологии. Если взять не с той зоны трансформации или неправильно перенести на стекло или в транспортную среду — всё, информативность падает. И лаборант тут уже не поможет.
Основные ошибки при заборе и почему они возникают
Самая частая проблема — недостаточный объём материала. Врач делает мазок, но щёточка или цитобраш контактирует только с поверхностью, не захватывая клетки из цервикального канала. Особенно это критично для ВПЧ-тестирования, ведь вирус может локализоваться именно в зоне трансформации. Бывает, используют устаревшие инструменты — деревянные шпатели, которые просто не способны эффективно собрать эндоцервикальные клетки. Результат — ложноотрицательный ответ, и пациентка уходит с ложным чувством безопасности.
Другая точка сбоя — подготовка пациента. Если забор проводится во время менструации или при выраженном воспалении, примесь крови и лейкоцитов может мешать анализу. Иногда сами женщины перед приёмом используют спринцевания или вагинальные свечи, что тоже искажает картину. Объяснять это каждый раз — обязанность врача, но в потоковом приёме про это частенько забывают.
И третий момент — техника переноса. При классической цитологии материал размазывают по стеклу, и тут важно сделать это тонким, равномерным слоем, без подсушивания. При жидкостной методике — сразу поместить головку щёточки в стабилизирующую жидкость, энергично прополоскать. Видела, как медсёстры, экономя время, просто кладут щёточку в контейнер, не выполняя активного перемешивания. Клетки остаются на щетинках, и в анализ попадает лишь часть материала.
Оборудование и расходники: на чём не стоит экономить
Здесь уже переходим к технической стороне. Качество инструментов для забора — это не просто вопрос удобства. Возьмём, к примеру, современные цитологические щёточки с разным дизайном головок (например, типа Cervex-Brush или комбинированные эндо/эктоцервикальные). Их конструкция позволяет одномоментно захватить материал и с эктоцервикса, и из цервикального канала. Это резко снижает вероятность пропуска атипичных клеток.
Особенно важно это для жидкостной цитологии, где дальнейшая обработка стандартизирована. Если используется система, например, ThinPrep или SurePath, то и щёточка, и транспортный контейнер должны быть совместимы с этой системой. Нельзя взять первую попавшуюся щётку, сунуть её в жидкость от другого производителя и ждать хорошего монослоя на стекле. Прецизионность начинается здесь.
К слову о совместимости. В последнее время на рынке появляются решения от компаний, которые предлагают комплексный подход к обновлению лабораторий. Как, например, ООО Хубэй Тайкан Медицинское Оборудование (сайт: https://www.cnhbtk.ru). Они позиционируют себя как специалисты в области цитопатологии, и их продуктовая линейка включает именно жидкостные тонкослойные цитологические системы и реагенты для скрининга рака шейки матки. Важен их акцент на экологическом и интеллектуальном обновлении лабораторий — это как раз про то, чтобы забор, транспортировка и подготовка препарата были звеньями одной цепочки, минимизирующей человеческий фактор. Использование таких комплексных систем, по моим наблюдениям, действительно снижает количество неинформативных образцов.
Транспортировка и хранение: невидимый этап, который всё портит
Представим, материал взят идеально. Что дальше? Контейнер может неделю пролежать в курьерской сумке или в холодильнике при неправильной температуре. Для жидкостных сред обычно есть чёткие требования: комнатная температура, без замораживания и прямого солнца. Нарушения в логистике — бич для периферийных клиник, которые отправляют образцы в региональные центры.
Был у меня показательный случай из практики. Из одного филиала постоянно приходили образцы с низкой клеточностью. Стали разбираться — оказалось, курьер забирал пробирки и складывал их в общий контейнер со льдом, предназначенный для других анализов. Жидкостная среда частично кристаллизовалась, клетки разрушались. После изменения протокола транспортировки проблема ушла.
Поэтому сейчас при выборе системы я всегда смотрю не только на саму щёточку и среду, но и на устойчивость этой среды к возможным колебаниям условий. Некоторые производители заявляют более широкий температурный диапазон стабильности, что для российской реальности с её расстояниями — критически важно.
Интерпретация результата и клиническое мышление
И вот результат пришёл. ВПЧ положительный, цитология — NILM. Или наоборот. Самая большая ошибка на этом этапе — слепо доверять бумажке. Забор материала для ВПЧ и цитологии — это, по сути, моментальный снимок. Вирусная нагрузка может колебаться, участок забора мог не попасть в зону с максимальной концентрацией вируса или дисплазией.
Поэтому всегда нужно соотносить результат с кольпоскопической картиной и анамнезом. Если есть визуальные изменения на шейке, а ВПЧ-тест отрицательный, я бы рекомендовала повторный забор через 6-12 месяцев, возможно, другим инструментом и с более тщательным подходом к зоне трансформации. Случаев, когда первичный тест ?не уловил?, а при контроле всё выявлялось, — немало.
Здесь также встаёт вопрос о выборе метода тестирования — просто ли это определение ДНК ВПЧ высокого риска или же генотипирование. Для молодых пациенток с хорошим иммунитетом и отрицательной кольпоскопией положительный ВПЧ 16/18 — это одно. А та же находка у женщины старше 45 с фоновыми заболеваниями — уже совсем другие риски и тактика. Сам по себе факт забора материала — лишь начало пути к диагнозу.
Выводы и практические рекомендации
Итак, что можно вынести для ежедневной работы? Во-первых, стандартизировать процедуру забора. Лучше использовать комбинированные щёточки, предназначенные для жидкостной цитологии, и строго следовать протоколу промывки в стабилизирующей жидкости. Не стесняться проводить мини-обучение для среднего медперсонала — от этого зависит всё.
Во-вторых, наладить чёткую логистику. Образцы должны храниться и транспортироваться в условиях, рекомендованных производителем тест-системы. Это банально, но именно на этом этапе происходит большинство потерь качества.
В-третьих, рассматривать результат в комплексе. Отрицательный ВПЧ при плохой кольпоскопии — не приговор тесту, а повод задуматься о качестве преаналитики. Иногда стоит обратиться к решениям, которые предлагают именно комплексный подход к преаналитическому этапу, как это делает, например, компания ООО Хубэй Тайкан Медицинское Оборудование, чья деятельность сфокусирована на модернизации патологических лабораторий. Их подход к созданию замкнутой системы — от набора материала до готового препарата — может минимизировать многие описанные риски.
В конечном счёте, грамотный забор материала для ВПЧ — это не просто технический протокол. Это акт клинического принятия решения, где от внимания к деталям зависит, получим ли мы информативный результат или потратим время и ресурсы впустую. И этот этап точно не тот, на котором стоит экономить или работать ?на авось?.
Соответствующая продукция
Соответствующая продукция
Самые продаваемые продукты
Самые продаваемые продукты-
 Декальцинирующий раствор
Декальцинирующий раствор -
 Среда для заливки в криостате
Среда для заливки в криостате -
 Преаналитические реагенты для патологических исследований
Преаналитические реагенты для патологических исследований -
 Раствор для окрашивания по Граму
Раствор для окрашивания по Граму -
 Раствор для окрашивания по Гимзе
Раствор для окрашивания по Гимзе -
 Фиксатор для тканей (альдегидсодержащий)
Фиксатор для тканей (альдегидсодержащий) -
 Архивные боксы для гистологических препаратов
Архивные боксы для гистологических препаратов -
 Микротом TKY-QPD (ручной)
Микротом TKY-QPD (ручной) -
 Раствор для окрашивания Г-Э
Раствор для окрашивания Г-Э -
 Оральная консервирующая жидкость
Оральная консервирующая жидкость -
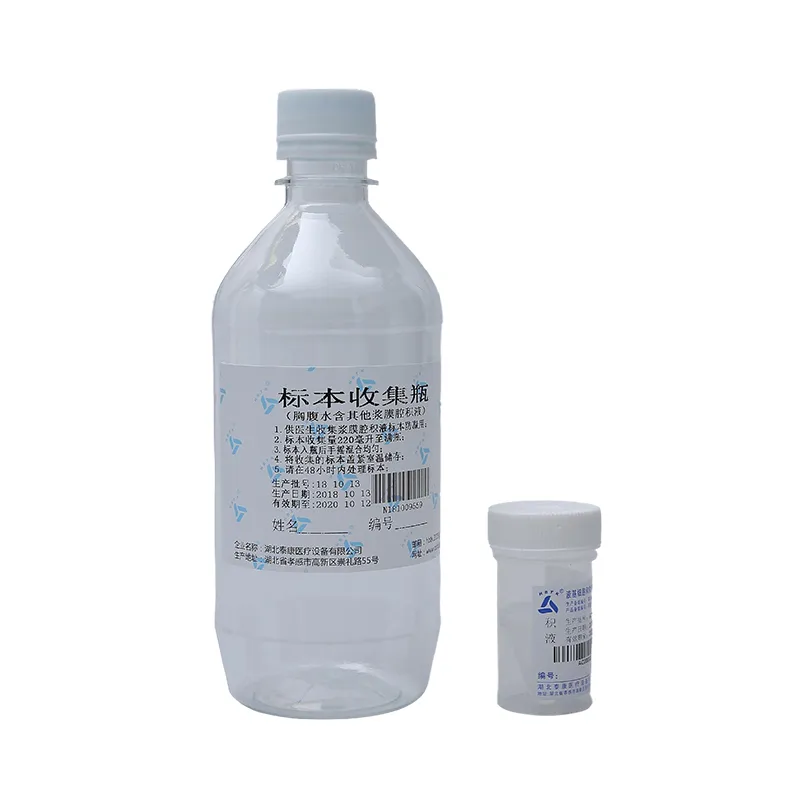 Специальная консервирующая жидкость для плеврального/асцитического выпота и лаважных жидкостей
Специальная консервирующая жидкость для плеврального/асцитического выпота и лаважных жидкостей -
 TP60A1TP100A1
TP60A1TP100A1
Связанный поиск
Связанный поиск- Окрасочно-монтажный аппарат для предметных стекол
- цитологический мазок впч
- цитологический мазок на флору
- Гематоксилин-Оранж G-EA50
- контейнер универсальный для транспортировки тары с образцами
- Ленточный тканевый дегидратор
- Экспресс-тканевой дегидратор для патологии
- Экологический патологический промывной раствор
- Нержавеющие заливочные матрицы для парафиновых срезов
- пластиковый контейнер для образцов