
Высокоточное стабильное окрашивание предметных стекол
Когда слышишь ?высокоточное стабильное окрашивание?, первое, что приходит в голову — это идеально ровные, контрастные, воспроизводимые изо дня в день препараты. Но на практике, между этим идеалом и реальным стеклом на столе гистолога лежит пропасть, которую многие недооценивают. Часто думают, что купил хороший автомат или дорогие красители — и все проблемы решены. А на деле начинается: то фон мутный, то ядра ?выцвели?, то партия на партию не похожа. И вот тут понимаешь, что точность и стабильность — это не про оборудование или химию по отдельности. Это про систему, где каждый шаг, от подготовки стекла до фиксации, должен быть под контролем. И даже мелочи, вроде качества воды для промывки или времени просушки, могут все испортить.
Где начинается стабильность: неочевидные отправные точки
Мой опыт — а я много лет работал с разными линейками — говорит, что гонку за стабильностью многие проигрывают еще на старте. Возьмем, к примеру, само предметное стекло. Казалось бы, оно инертное. Но его смачиваемость, чистота, наличие силиконового покрытия или его отсутствие — это фундамент. Если основа кривая, никакой, даже самый совершенный, протокол окрашивания не даст того самого высокоточного стабильного окрашивания. Мы как-то получили партию стекол с едва заметным производственным загрязнением. На вид — идеальные. А при окрашивании по Папаниколау клетки местами просто не адгезировали, получались ?проплешины?. Стабильность всей серии была нулевой.
Или фиксация. Спиртовая, аэрозольная, цитологическим спреем. Каждый метод диктует свои условия для последующих этапов. Ранняя фиксация, поздняя, неполная — это все аукнется на интенсивности окраски ядер. Особенно критично для жидкостной цитологии, где важно сохранить морфологию в тонком слое. Тут без четкого, выверенного до секунд протокола не обойтись. Стабильность рождается из повторяемости, а повторяемость — из жесткой дисциплины на каждом, даже самом простом, этапе.
И вода. Дистиллированная, деионизированная, типа I. Ее pH, электропроводность. Если в лаборатории жесткая вода идет на промывку, можно забыть о чистом фоне. Соли дают осадок, который окрашивается и маскирует детали. Мы перешли на использование воды, подготовленной системой очистки с контролем сопротивления, и количество артефактов на стеклах упало в разы. Это тот базис, о котором не пишут в ярких рекламных буклетах к окрашивающим станциям, но который в лаборатории решает все.
Оборудование и реагенты: тандем, а не волшебная палочка
Автоматические окрашивающие машины — это, конечно, огромный шаг к стабильности. Они убирают человеческий фактор, выдерживают время, температуру, последовательность. Но и тут есть свои ?но?. Возьмем, к примеру, аппараты для жидкостной цитологии. Их задача — не только нанести монослой, но и обеспечить идеальные условия для последующего окрашивания. Если в самом аппарате, например, нестабилен вакуум или скорость вращения, слой получается неравномерным — толще по краям, тоньше в центре. И любое, даже самое высокоточное окрашивание, эту проблему не скроет, а лишь подчеркнет.
Здесь стоит упомянуть решения, которые работают именно на создание такой интегрированной системы. Например, компания ООО Хубэй Тайкан Медицинское Оборудование (сайт: https://www.cnhbtk.ru), которая как раз фокусируется на комплексном обновлении патологических лабораторий. Их подход мне близок: они не просто продают препарирователи для тонкослойных мазков, а думают о всей цепочке — от взятия образца до окрашенного стекла. Их оборудование и реагенты для скрининга, включая окрашивание, часто проектируются с учетом взаимной совместимости. Это важно, потому что когда ты используешь пресс для мазков от одного производителя, реагенты от второго, а автомат для окраски от третьего, добиться предсказуемости очень сложно. Производитель, который контролирует больше этапов, может гарантировать лучшую стабильность на выходе.
Но даже с лучшим оборудованием реагенты — это отдельная песня. Партионные вариации есть у всех. Ключ — в контроле входящего качества. Мы вводили правило: каждая новая партия красителей, особенно гематоксилина, тестируется на контрольных стеклах параллельно со старой. Сравниваем оттенок ядер, четкость хроматина, цвет цитоплазмы. Малейшие отклонения — и мы уже знаем, нужно ли корректировать время окраски для этой партии. Это рутина, но это и есть та самая практическая работа по обеспечению стабильности, которой нет в инструкциях.
Протоколы: искусство баланса между идеалом и реальностью
В книгах протоколы выглядят строго и незыблемо: 5 минут в гематоксилине, 1 минута в кислом спирте, 5 минут в эозине. В жизни все иначе. Гематоксилин ?стареет? по мере окисления и использования, его активность падает. Если слепо держать 5 минут по таймеру, через месяц ядра будут бледными. Приходится развивать ?чувство цвета?. Смотришь на контрольное стекло после дифференцировки — и понимаешь, нужно ли добавить 15 секунд или, наоборот, сократить. Это и есть та самая ?высокая точность?, которая достигается не машиной, а опытом. Машина дает повторяемость, а человек-технолог вносит поправку на изменяющиеся условия, обеспечивая тем самым истинную стабильность результата.
Особенно капризна дифференцировка. Передифференцировал — потерял детализацию ядра, важную для диагностики дисплазии или злокачественности. Недодифференцировал — фон темный, клетки плохо читаются. Здесь нет универсального совета, кроме постоянного использования контрольных препаратов. Мы всегда в каждой серии окрашиваем одно-два контрольных стекла с известной патологией. Это наш главный ориентир.
Еще один момент — температура в лаборатории. Летом, в жару, реакции идут быстрее. Зимой, если лаборатория прохладная, красители могут работать медленнее. Автомат, конечно, нивелирует это, если у него есть термостатируемая камера. Но если окрашивание ручное или полуавтоматическое, об этом факторе забывать нельзя. Пришлось как-то даже график корректировок времени окрашивания в зависимости от сезонной температуры в помещении составить. Мелочь? Да. Но без учета таких мелочей о стабильности можно только мечтать.
Контроль качества: не для отчета, а для диагноза
Внутрилабораторный контроль качества окрашивания — это не та бумажка, которую инспектору показывают. Это ежедневный инструмент. Помимо контрольных стекол, мы ввели оценку по внутренним критериям. У нас есть чек-лист: чистота фона, контрастность ядра/цитоплазмы, интенсивность окраски ядер, отсутствие артефактов (осадок, полосы). Каждую партию окрашенных стекол, особенно для важных исследований, вроде скрининга шейки матки, выборочно оценивает старший технолог. Если видит тенденцию к отклонению — например, фон стал чаще с легкой розовинкой — это сигнал проверить воду, свежесть спиртов для обезвоживания или время промывки.
Для жидкостной цитологии, которой занимается ООО Хубэй Тайкан, контроль еще строже. Тонкий слой менее ?прощает? ошибки. Неполная фиксация или неидеальное окрашивание видны как на ладони. Поэтому в их комплексах для скрининга, насколько я знаю, большое внимание уделяется именно стандартизации преаналитики и аналитики как единого процесса. Ведь их цель — стабильное окрашивание не как самоцель, а как условие для точного и раннего выявления патологии, будь то в гинекологии или в урологии (тут вспомним их реагенты для скрининга по моче).
Раз в квартал мы проводим более глубокий анализ — окрашиваем один и тот же блок срезов в течение недели, в разные смены, разными технологами. Потом смотрим все стекла под микроскопом вместе с патологоанатомом. Это бесценно. Патолог сразу говорит: ?Вот на этих стеклах я увереннее ставлю оценку, а вот эти заставляют всматриваться?. Эти обратные связи и есть главный двигатель для улучшения всего процесса.
Ошибки и тупики: чему учат неудачи
Было у нас и неудачное внедрение одного автоматического окрашивателя. Машина была современная, дорогая, с цифровым управлением. Но ее программа промывки между красителями была слишком экономной по расходу спиртов и ксилола. В теории — экономия реагентов. На практике — постепенный перенос красителей из ванны в ванну, особенно эозина в ксилол. Через месяц работы фон на стеклах приобрел стойкий розоватый оттенок. Пришлось срочно менять протокол, увеличивать объем промывок, что свело на нет всю экономию. Вывод: любая автоматизация требует валидации под свои конкретные реагенты и условия. Слепо доверять заводским настройкам нельзя.
Другой случай связан с попыткой сэкономить на обезвоживающих спиртах. Перешли на более дешевые, неабсолютные. Результат — мутный фон, будто на стекле легкая дымка. Оказалось, остатки воды в спиртах плохо взаимодействовали с ксилолом и средой для заключения. Пришлось вернуться к проверенному поставщику. Эта история окончательно убедила меня, что в гистологии и цитологии на реагентах для проводки и окрашивания экономить — себе дороже. Рискнуть качеством препарата, от которого зависит диагноз, — непозволительная роскошь.
Сейчас, оглядываясь назад, понимаю, что путь к высокоточному стабильному окрашиванию предметных стекол — это не пункт назначения, а постоянное движение. Это ежедневная внимательность к деталям, готовность проверять и перепроверять, адаптировать протоколы и не бояться учиться на своих ошибках. Это когда ты смотришь на готовое стекло и не просто видишь окрашенные клетки, а понимаешь всю историю, которая стоит за этой картинкой: от качества стекла и фиксации до последней капли ксилола. И именно такая, неидеальная, но вдумчивая работа в лаборатории в итоге и дает ту самую стабильность и точность, на которые может положиться врач-патолог. Все остальное — просто красивые слова.
Соответствующая продукция
Соответствующая продукция
Самые продаваемые продукты
Самые продаваемые продукты-
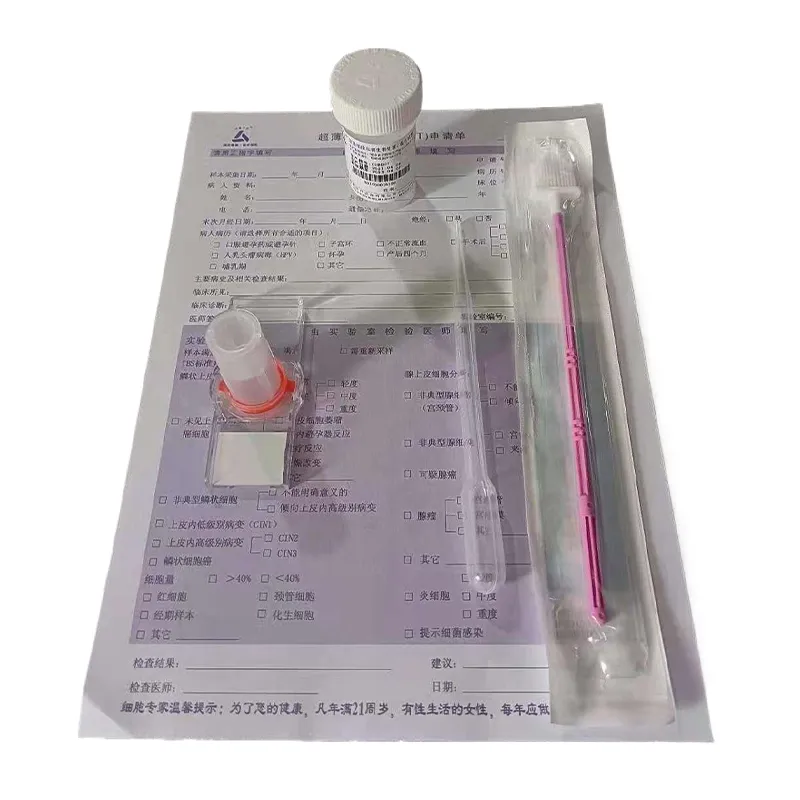 Ранний скрининг рака шейки матки
Ранний скрининг рака шейки матки -
 Раствор для окрашивания гинекологических мазков
Раствор для окрашивания гинекологических мазков -
 Ранний скрининг рака лёгких
Ранний скрининг рака лёгких -
 Ленточный тканевый дегидратор
Ленточный тканевый дегидратор -
 Архивные боксы для гистологических препаратов
Архивные боксы для гистологических препаратов -
 Одноразовые микротомные лезвия
Одноразовые микротомные лезвия -
 Жидкость для подготовки гистологических образцов
Жидкость для подготовки гистологических образцов -
 Носоглоточная консервирующая жидкость
Носоглоточная консервирующая жидкость -
 Криомикротом
Криомикротом -
 Аппарат для расправления и фиксации гистологических срезов
Аппарат для расправления и фиксации гистологических срезов -
 Фиксатор для биопсийного материала (безальдегидный)
Фиксатор для биопсийного материала (безальдегидный) -
 Жидкостный тонкослойный цитологический пресс
Жидкостный тонкослойный цитологический пресс
Связанный поиск
Связанный поиск- окраска цитологических мазков по папаниколау
- Забор материала для ВПЧ (гинекология)
- Раствор для окрашивания по Граму
- Раствор для высокоточного стабильного окрашивания
- виды цитологических мазков
- Ротационный ручной микротом
- цитологическое исследование мазка костного мозга
- цитологический мазок жидкостной
- Раствор для очистки рабочих столов и ванн (ручной распылитель) 200 мл, 5 л
- Полностью автоматизированный интегрированный аппарат для приготовления и окрашивания предметных стекол












