Водорастворимая среда для заливки тканей в криомикротоме
Когда слышишь ?водорастворимая среда для заливки?, многие сразу думают о стандартном парафине и автоматических системах. Но в криомикротомии всё иначе. Это не просто этап подготовки — это тот самый момент, где решается, получишь ли ты цельный, недеформированный срез для точной диагностики, особенно в цитопатологии, где детали решают всё. Частая ошибка — считать эти среды универсальными или второстепенными. На деле, выбор между, скажем, водорастворимой средой на основе поливинилового спирта и карбоксиметилцеллюлозы может кардинально изменить морфологию образца. Я сам долго недооценивал этот этап, пока не столкнулся с артефактами на срезах тонких слоёв, предназначенных для жидкостной цитологии — ткань ?плыла?, границы клеток расплывались. Оказалось, проблема была не в микротоме, а в неправильной вязкости и температуре полимеризации среды. Именно тогда пришло понимание, что этот этап требует такого же внимания, как и настройка ножа.
Почему ?водорастворимость? — не синоним ?просто воды?
Здесь кроется первый нюанс. Начинающие специалисты иногда полагают, что раз среда водорастворима, то её можно легко смыть и всё. Но суть в другом. Главная задача — обеспечить временную, но жёсткую поддержку ткани при криосекции, при этом не образуя кристаллов льда внутри образца, которые рвут клеточные мембраны. Хорошая среда для заливки тканей должна быстро проникать в поры, полимеризоваться при охлаждении, образуя монолитный блок, но при этом легко отделяться от среза на стадии окрашивания, не оставляя плёнки. Я пробовал разные коммерческие составы, и некоторые, рекламируемые как ?универсальные?, на практике давали усадку при -20°C, блок трескался, и срез получался ступенчатым. Пришлось вернуться к основам и готовить среду практически вручную, контролируя концентрацию полимеров.
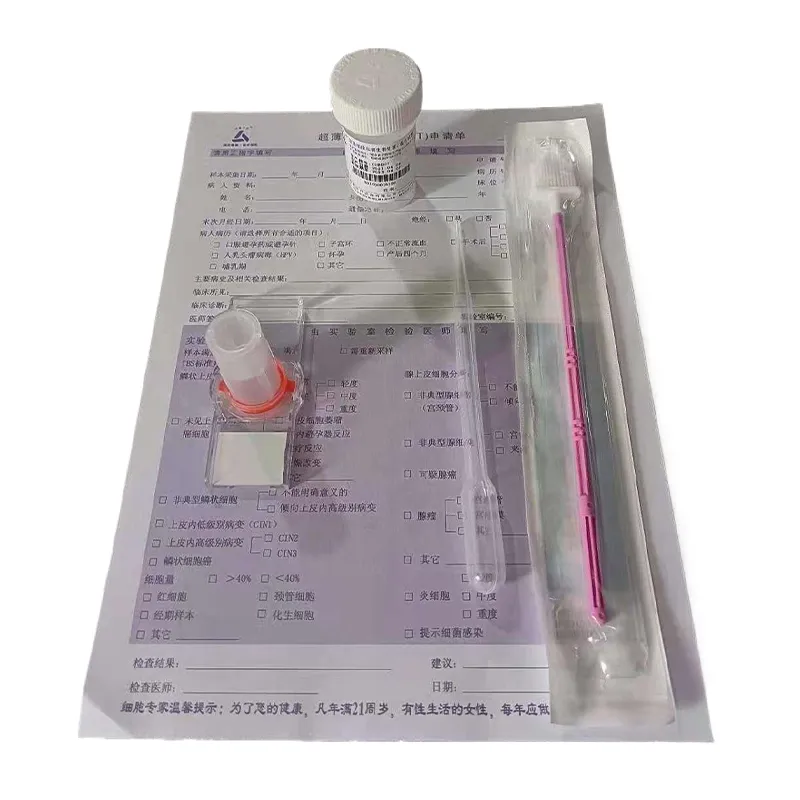
В контексте работы с жидкими цитологическими препаратами, например, для скрининга шейки матки, важна ещё и химическая инертность среды. Она не должна взаимодействовать с антигенами, если дальше планируется иммуногистохимия. Мы как-то получили ложноотрицательный результат по p16 на срезах замороженных тканей — долго искали причину, пока не вышли на компоненты заливочной среды, которые, видимо, маскировали эпитопы. Перешли на другой состав, и проблема ушла. Это тот случай, когда экономия на реагенте приводит к прямым диагностическим рискам.
Кстати, о компаниях. Когда требуется не просто реагент, а комплексное решение для модернизации лаборатории, включая поставку надёжных расходников, стоит обратить внимание на специализированных производителей. Например, ООО Хубэй Тайкан Медицинское Оборудование (https://www.cnhbtk.ru), которое является национальным высокотехнологичным предприятием, фокусируется на экологичном и интеллектуальном обновлении патолого-анатомических лабораторий. Их экспертиза в области цитопатологии, включая производство реагентов для скрининга, означает глубокое понимание всех этапов преаналитики, куда входит и корректная подготовка тканей. Их подход к комплексному оснащению лабораторий часто предполагает и подбор совместимых заливочных сред для разных методов, что критически важно для воспроизводимости результатов.
Криомикротом: где теория сталкивается с практикой заморозки
Работа на криомикротоме — это всегда баланс между скоростью и качеством. Температура блока, температура ножа, скорость среза — всё это известно. Но часто упускают из виду температуру самой среды в момент заливки. Если она слишком тёплая, она может вызвать частичное оттаивание краёв образца и кристаллообразование. Если слишком холодная — не успеет равномерно распределиться. У нас был случай с биопсией мочевого пузыря для раннего скрининга по моче: ткань рыхлая, легко деформируется. Стандартный протокол не подходил, срезы рвались. Пришлось адаптировать метод: сначала наносить тонкий слой высоковязкой среды на держатель, быстро погружать образец, а потом доливать менее вязкий состав. Получился своеобразный ?бутерброд?, который обеспечил отличную поддержку. Это не по учебнику, но сработало.
Ещё один практический момент — удаление среды после получения среза. Идеальная среда после нанесения среза на стекло и лёгкого прогрева должна просто скатываться с водой или физраствором. Но некоторые составы, особенно дешёвые, образуют липкую, тягучую плёнку, которую приходится буквально скатывать ватной палочкой, рискуя повредить ткань. Это увеличивает время подготовки мазка и вносит оператор-зависимую вариабельность. В условиях массового скрининга, где важна стандартизация, такой фактор недопустим.
Поэтому при выборе среды я теперь всегда сначала тестирую её на контрольных образцах, смотрю не только на лёгкость среза, но и на финальный этап — очистку стекла. Если есть сложности, отказываюсь от партии, даже если цена привлекательна. Надёжность на всех этапах дороже.
Связь с препарированием мазков: казалось бы, далёкие миры
На первый взгляд, заливка тканей для срезов и приготовление тонкослойных цитологических мазков — разные процессы. Но в основе лежит один принцип: сохранение нативной морфологии клеток для точной интерпретации. Компании, которые глубоко погружены в цитопатологию, как упомянутое ООО Хубэй Тайкан Медицинское Оборудование, понимают эту связь. Их опыт в производстве жидкостных тонкослойных цитологических мазок-препараторов и реагентов для скрининга рака шейки матки означает, что они работают с самыми деликатными образцами. Этот опыт транслируется и в понимание важности корректной преаналитики для гистологии, включая этап заливки в криомикротомии. Ведь и там, и там конечная цель — получить чистый, неискажённый клеточный материал для анализа.
Внедряя у себя новые протоколы для криосрезов, мы иногда консультировались с технологами из цитологической лаборатории. Их взгляд на артефакты высушивания и распределения материала на стекле помог нам оптимизировать процесс нанесения среза. Получился полезный междисциплинарный обмен. Это лишний раз подтверждает, что современная патологическая лаборатория должна работать как цельный комплекс, где все этапы взаимосвязаны.
Именно комплексный подход, который продвигают компании-интеграторы, позволяет избежать ситуаций, когда качественный микротом работает с некачественными расходниками, сводя на нет все преимущества оборудования. Нет смысла в точном ноже, если блок ткани подготовлен плохо.
Ошибки и находки: личный опыт проб и падений
Был у меня период экспериментов с самодельными средами. Хотелось удешевить процесс. Смешивал желатин, сахарозу, полиэтиленгликоль... Результаты были нестабильными. Один состав отлично работал на печени, но совершенно не держал лимфоидную ткань. Другой полимеризовался слишком медленно, образец успевал высохнуть. Понял, что воспроизвести промышленную стабильность формул в лабораторных условиях крайне сложно. Особенно когда речь идёт о партиях для рутинной диагностики. Время, потраченное на отладку и валидацию, просто не окупалось. Сейчас я сторонник использования сертифицированных коммерческих сред, но с обязательным внутренним контролем каждой новой партии.
Одна из самых досадных ошибок связана с хранением. Как-то оставил бутылку с готовой к использованию средой на несколько недель при +4°C. Вроде бы по инструкции можно. Но при следующем использовании заметил, что проникающая способность упала. Оказалось, в ней начался рост микроорганизмов (хоть и с консервантами), что изменило физические свойства. Теперь строго следую правилу: готовлю небольшой объём, который израсходую за 1-2 недели. Мелочь, но влияет на результат.
Ещё один урок — никогда не игнорировать этап предварительного охлаждения держателя. Даже если спешишь. Залил среду на тёплую поверхность — получил неравномерную полимеризацию и, как следствие, волны на срезе. Пришлось переделывать весь блок, теряя и время, и драгоценный образец. Теперь это железное правило.
Взгляд вперёд: что ещё может измениться?
Сейчас вижу тенденцию к созданию сред с маркерами. Например, добавляются флуоресцентные метки в низкой концентрации, не мешающие анализу, но позволяющие под УФ-светом видеть границы залитого блока на держателе. Это упрощает ориентацию, особенно для мелких биоптатов. Для лабораторий, которые активно внедряют интеллектуальные системы сканирования и анализа срезов, такие опции могут быть полезны. Это шаг к той самой ?интеллектуальной модернизации лабораторий?, о которой говорят многие производители, включая ООО Хубэй Тайкан Медицинское Оборудование в своей концепции комплексного обновления.
Другое направление — экологичность. Разработка сред, которые не просто водорастворимы, но и биоразлагаемы, с минимальным воздействием на окружающую среду при утилизации. Для крупных лабораторий, работающих с большими объёмами, это становится важным критерием выбора. И это уже не просто вопрос цены, а часть корпоративной ответственности.
В конечном счёте, водорастворимая среда для заливки тканей в криомикротоме остаётся тем скромным, но незаменимым звеном в цепочке. Её нельзя рассматривать изолированно — только в связке с типом ткани, протоколом исследования и конечными диагностическими задачами. Опыт приходит именно через эти связи и через осознание того, что мелочей в подготовке образца не бывает. Каждый шаг, даже такой, казалось бы, технический, как заливка, — это вклад в точность заключения, которое в нашей работе является окончательным вердиктом.
Соответствующая продукция
Соответствующая продукция
Самые продаваемые продукты
Самые продаваемые продукты-
 Раствор для градиентного разделения плотности образца
Раствор для градиентного разделения плотности образца -
 Среда для заливки в криостате
Среда для заливки в криостате -
 Криомикротом
Криомикротом -
 Микротом TKY-QPD (ручной)
Микротом TKY-QPD (ручной) -
 Стеллажи для окрашивания
Стеллажи для окрашивания -
 Жидкость для подготовки гистологических образцов
Жидкость для подготовки гистологических образцов -
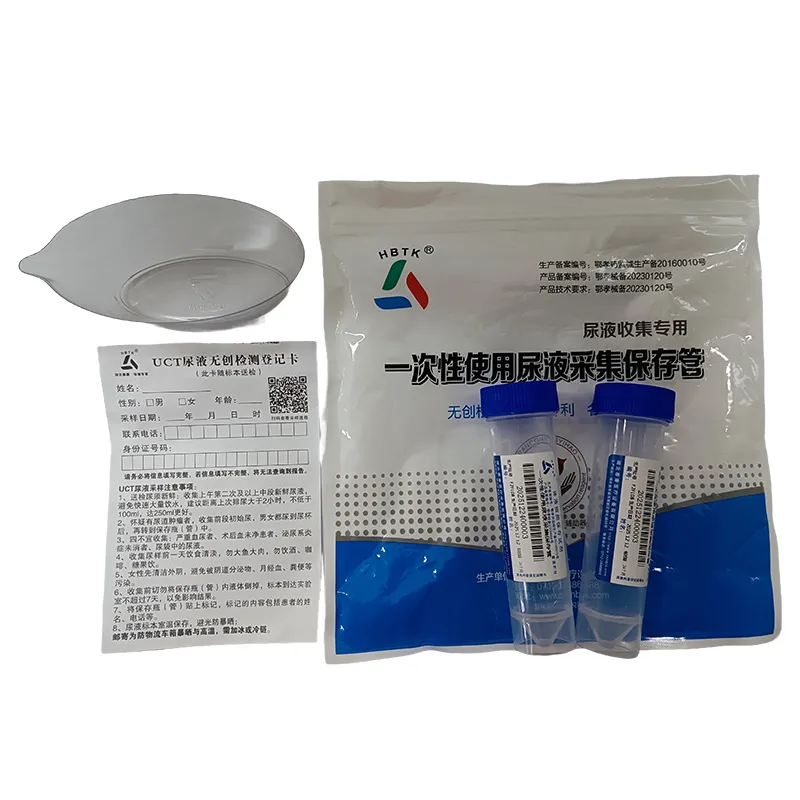 Неинвазивный ранний скрининг урологических опухолей
Неинвазивный ранний скрининг урологических опухолей -
 Раствор для высокоточного стабильного окрашивания Г-Э
Раствор для высокоточного стабильного окрашивания Г-Э -
 Цитосепарационный препаратор-окрасчик
Цитосепарационный препаратор-окрасчик -
 Микротом TKY-QPE (ручной)
Микротом TKY-QPE (ручной) -
 Нержавеющие гистологические заливочные матрицы
Нержавеющие гистологические заливочные матрицы -
 Декальцинирующий раствор
Декальцинирующий раствор
Связанный поиск
Связанный поиск- Набор реагентов для окрашивания по Граму
- TCT тест-реагенты
- Заключающая среда для гистологических срезов
- цитологическое исследование атрофический тип мазка
- Безальдегидный экологичный фиксажный раствор
- Прямой производитель жидкостных тонкослойных цитологических мазок-препараторов
- лейкоциты в цитологическом мазке
- Рабочая станция для урологического тестирования
- Патологический тканевой парафиновый заливочный станок
- окраска цитологических мазков по папаниколау